L'acido urico: fatti e misfatti
Enrico Bologna
Specialista in Medicina Interna, Gastroenterologia e Patologia generale.
Già Primario Ospedale Fatebenefratelli, Isola Tiberina, Roma.
Libero docente in Patologia Medica, Università di Roma “Sapienza”.
La gotta, conseguenza più nota dell'alterato metabolismo delle purine, è il risultato dell'azione di cristalli di urato monosodico monoidrato la cui formazione nei tessuti per eccessiva concentrazione nel sangue, agendo su particolari recettori presenti sui monociti (Toll-Like Receptors, TLR) attiva un complesso citoplasmatico denominato inflammasome il cui prodotto finale è rappresentato da Interleukina-1β (IL-1β) (11,25)
L'associazione della gotta con il diabete mellito e con varie malattie cardiovascolari e renali, segnalata già alla fine del 1800, dalla metà del secolo scorso è tornata ad essere oggetto di numerose ricerche epidemiologiche e sperimentali, parte delle quali hanno portato sostegno all'ipotesi di un rapporto causale fra iperuricemia e varie condizioni quali ipertensione arteriosa, sindrome metabolica, coronaropatie, malattia cerebrovascolare, demenza vascolare, preeclampsia, nefropatie, aumento dei marker di infiammazione e post-menopausa. Si tratta di una ipotesi controversa, e infatti nelle attuali linee guida l'uricemia non viene inclusa tra i fattori di rischio cardiovascolare richiedenti trattamento. Il problema viene tuttavia considerato meritevole di approfondimento, come dimostrato anche dall'attenzione del Public Healt Service statunitense che ha finanziato una rassegna sul tema, recentemente pubblicata sul New England Journal of Medicine a cura di D.J. Feig & al (14)
Anche la diminuita concentrazione plasmatica di acido urico viene chiamata in causa nella patogenesi di alcune affezioni: si tratta di varie malattie neurodegenerative, fra cui sclerosi multipla, neurite ottica, malattie di Parkinson e di Alzheimer, lesioni midollari. Perciò, accanto ai trattamenti dietetici e farmacologici volti a ridurre l'uricemia nei soggetti gottosi ed anche in quelli con ipertensione arteriosa e con altre malattie cardiovascolari o renali, sono stati proposti e/o attuati trattamenti farmacologici destinati a far aumentare l'uricemia (mediante somministrazione di inosina, precursore di acido urico) in soggetti con sclerosi multipla e con lesioni del midollo spinale (24)
Nella maggior parte dei mammiferi il metabolismo delle basi puriniche presenti nel DNA, adenina e guanina, termina con la formazione di allantoina, sostanza altamente idrosolubile, mentre il suo precursore acido urico, meno solubile, non supera nel plasma la concentrazione di 2 mg/dL. Solo nell'uomo e nelle grandi scimmie (Chimpanzé, Gorilla, Orangutan e Gibbone) i valori sono più elevati (4-7 mg/dL) (Tab.I).
Tab.I
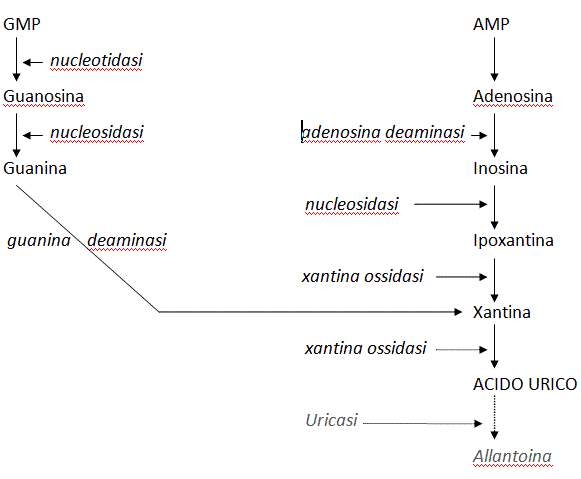 Questa diversità dipende dalla mancanza, nell'uomo e nelle grandi scimmie, del gene dell'enzima urato-ossidasi (uricasi). Secondo studi di paleontologia genetica la perdita di questo gene si deve far risalire al Miocene, cioè al periodo compreso fra 10 e 20 milioni di anni fa. Gli stessi studi hanno permesso di stabilire che la perdita dell'uricasi è avvenuta, nelle specie sopra indicate, in momenti diversi di questa era geologica. E' stato ipotizzato che questo evento abbia conferito un vantaggio ai fini della sopravvivenza di mammiferi che si alimentavano con cibi vegetali, e quindi poveri di sale, e che stavano assumendo la posizione eretta; in altri termini, l'aumento dell'uricemia conseguente alla scomparsa dell'uricasi nei primati viene interpretata come un fenomeno favorevole in quanto capace di compensare l'iponatremia e quindi utile per mantenere o elevare la pressione arteriosa rendendola adeguata all'ortostatismo (44). Questa ipotesi è suffragata da osservazioni sperimentali e cliniche. Le prime sono rappresentate dalla riduzione pressoria che si manifesta in topi trattati con Allopurinolo e che è di entità analoga a quella provocata negli stessi animali dalla dieta iposodica; inoltre dall'aumento pressorio indotto, sempre nei topi, dalla somministrazione di un inibitore dell'uricasi (acido ossonico), aumento che viene inibito dalla concomitante somministrazione di uricasi. Una conferma clinica è rappresentata dalla riduzione della pressione arteriosa che il trattamento con Allopurinolo determina in adolescenti con ipertensione essenziale e con uricemia pari o superiore a 6 mg/dL (13, 27)
Questa diversità dipende dalla mancanza, nell'uomo e nelle grandi scimmie, del gene dell'enzima urato-ossidasi (uricasi). Secondo studi di paleontologia genetica la perdita di questo gene si deve far risalire al Miocene, cioè al periodo compreso fra 10 e 20 milioni di anni fa. Gli stessi studi hanno permesso di stabilire che la perdita dell'uricasi è avvenuta, nelle specie sopra indicate, in momenti diversi di questa era geologica. E' stato ipotizzato che questo evento abbia conferito un vantaggio ai fini della sopravvivenza di mammiferi che si alimentavano con cibi vegetali, e quindi poveri di sale, e che stavano assumendo la posizione eretta; in altri termini, l'aumento dell'uricemia conseguente alla scomparsa dell'uricasi nei primati viene interpretata come un fenomeno favorevole in quanto capace di compensare l'iponatremia e quindi utile per mantenere o elevare la pressione arteriosa rendendola adeguata all'ortostatismo (44). Questa ipotesi è suffragata da osservazioni sperimentali e cliniche. Le prime sono rappresentate dalla riduzione pressoria che si manifesta in topi trattati con Allopurinolo e che è di entità analoga a quella provocata negli stessi animali dalla dieta iposodica; inoltre dall'aumento pressorio indotto, sempre nei topi, dalla somministrazione di un inibitore dell'uricasi (acido ossonico), aumento che viene inibito dalla concomitante somministrazione di uricasi. Una conferma clinica è rappresentata dalla riduzione della pressione arteriosa che il trattamento con Allopurinolo determina in adolescenti con ipertensione essenziale e con uricemia pari o superiore a 6 mg/dL (13, 27)
Tra le recenti acquisizioni sul ruolo dell'acido urico in patologia umana merita di essere menzionata quella relativa alla capacità immunostimolante di questa molecola. L' ipotesi è stata avanzata considerando che il potenziamento dei vaccini viene ottenuto con l'associazione di adiuvanti che agiscono previo legame ai recettori TLR dei monociti, già ricordati per il ruolo rivestito nella risposta immunitaria, che sono idonei a riconoscere regioni strutturali delle molecole di origine batterica ed a stabilire un legame con esse ma non con quelle di provenienza umana. Il riconoscimento da parte di questi recettori è determinante perché l'antigene possa indurre attivazione dei linfociti T; in assenza di esso, infatti, il contatto con l'antigene può determinare un effetto di tolleranza anziché di stimolo immunitario. Un adiuvante noto per la capacità di attivare i linfociti T è il citosol proveniente da cellule di mammiferi danneggiate. Le componenti citosoliche dotate di attività adiuvante sono due: una sostanza ad elevato peso molecolare, la cui natura non è stata ancora definita; l'altra è l'acido urico (26, 31). Si ritiene pertanto che la morte cellulare programmata dia inizio ad un processo di degradazione delle purine con produzione locale di acido urico, che agirebbe come "segnale di danno" diretto al sistema immunitario. Anche con questo meccanismo la presenza di acido urico conferirebbe una protezione per la sopravvivenza (3, 34) Acido urico, inoltre, è il principale antiossidante naturale presente nel sangue circolante ed è capace di prevenire la tossicità delle forme reattive dell'ossigeno rallentando la degradazione di superossidodismutasi e prevenendo in tal modo la formazione di perossinitrito (ONOO—) a partire da monossido di azoto (NO) e da radicale superossido (O2.—) ). Al perossinitrito viene attribuita la capacità di intervenire nella patogenesi di numerose condizioni morbose quali malattie cardiovascolari, stati infiammatori, neoplasie, ictus cerebrale, diabete mellito e malattie neurodegnerative. Il ruolo protettivo dell'attività antiossidante di acido urico è considerate preminente soprattutto nei confronti di queste ultime (2,9,29,40).
Acido urico è di provenienza sia endogena, cioè da sintesi de novo e da catabolismo degli acidi nucleici (500-600 mg/die), sia alimentare (100-200 mg/die). L'eliminazione dipende per circa il 75% dal rene e per il restante da uricolisi batterica intestinale. In condizioni normali il pool di acido urico è circa 1.200 mg, circa la metà nella donna; il 60% del pool è soggetto a ricambio nelle 24 ore. Acido urico è un acido debole, con pKa 5,75 nel sangue e 5,25 nelle urine. A pH 7,4 la reazione acido urico↔urato + H+ è spostata a destra; pertanto la maggior parte di acido urico circola nel sangue come ione urato.
L'eliminazione renale di acido urico è un fenomeno complesso: la molecola, idrosolubile e con basso legame plasmaproteico (circa 5%) è liberamente filtrata dal glomerulo. Almeno il 90% della quota filtrata va incontro a riassorbimento attivo nel tubulo prossimale, soprattutto ad opera del trasportatore URAT-1. In segmenti successivi del tubulo hanno luogo fenomeni di secrezione e di riassorbimento postsecretivo, anch'essi attivi e in buona parte sensibili a molteplici sostanze e farmaci. Il risultato netto di questi processi è l'eliminazione con le urine del 7-12% del carico filtrato.
Una definizione di iperuricemia, difficile sul piano statistico per le differenze nella distribuzione delle concentrazioni di urato nelle diverse popolazioni, è più semplice e clinicamente utile se posta in base a criteri fisico-chimici. A pH fisiologico ed a normale temperatura il limite di solubilità dell'urato è 6,8 mg/dL. Questo valore si riferisce alla misura effettuata con i metodi automatici enzimatici (uricasi), mentre con i metodi colorimetrici il valore stesso è più alto di circa 1 mg/dL. Se il limite di solubilità viene superato il pool di acido urico si espande a causa della deposizione di urato che precipita nei tessuti sotto forma di microcristalli la cui presenza determina fenomeni infiammatori nei tessuti molli anche in forma visibile (tofi), nei reni e nelle articolazioni dove, per lo più in concomitanza con meccanismi fisici, può scatenare la tipica manifestazione artritica acuta.
Le principali condizioni morbose provocate dalla deposizione di cristalli di urato sono la gotta, la litiasi urica e la nefropatia uratica acuta e cronica. L'incidenza annuale di manifestazioni gottose è correlata all'entità dell'iperuricemia: dal 4,9% per uricemie oltre i 9 mg/dL allo 0,1% per valori inferiori a 7 mg/dL. Una netta correlazione esiste anche tra valori uricemici, uricuria e calcolosi uratica: nei soggetti la cui uricuria giornaliera supera i 1.100 mg la frequenza di calcolosi uratica è del 50% (42), Meno stretti appaiono i rapporti fra uricemia e nefropatia uratica, che nella forma cronica, insorge solo nei rari soggetti con uricemia persistentemente superiore a 13 mg/dL nell'uomo e 10 mg/dL nella donna, mentre in forma acuta è possibile conseguenza della citolisi tumorale.
La causa dell'iperuricemia è rappresentata, nell'85-90% dei casi, da ridotta escrezione renale per cause patologiche o per effetto di farmaci; fanno parte di questa percentuale anche le forme indotte da alimenti (carne o pesce) in quanto l'iperuricemia consegue alla incapacità dei reni di eliminare un eccessivo carico purinico esogeno. Infatti i soggetti ipoescretori hanno una escrezione di urato quantitativamente normale, che però è ottenuta a valori più elevati di uricemia.
Nel 10-15% dei casi l'iperuricemia dipende da sovraproduzione di acido urico dovuta a difetti congeniti della sintesi delle purine (iperattività dell'enzima fosforibosilpirofosfatosintetasi, ovvero deficit di ipoxantina-guanina-foìsforibosiltrasferasi) o da condizioni che comportano accelerato ricambio cellulare (malattie proliferative, trattamenti citolitici). In una quota non trascurabile di questi casi coesiste un deficit relativo della escrezione.
Nei paesi occidentali l'uricemia media è in progressivo aumento: nella popolazione maschile degli USA il valore è passato da meno di 3,5 mg/dL degli anni '20 a 6,0 – 6,5 mg/dL degli anni '70 ed è in ulteriore aumento. Nella donna in età fertile i valori sono più bassi per l'effetto uricosurico degli estrogeni.
Il recente progressivo aumento dell'uricemia viene messo in rapporto con la crescente diffusione di sovrappeso e obesità e dall'aumentato consumo di alimenti ricchi di purine (soprattutto carni e in minor misura pesce, mentre i latticini sembrano svolgere un'azione protettiva), di bevande alcooliche (soprattutto liquori e birra, mentre il vino sembra avere un effetto modesto o nullo) e di bibite dolcificate con fruttosio (43). La responsabilità dell'alcool dipende dal fatto che nei processi di biotrasformazione esso può dar luogo alla formazione di lattato, che compete con l'acido urico per l'eliminazione renale; la birra scura e alcuni vini rossi, inoltre, contengono purine. Diverso è il meccanismo relativo al fruttosio: questo zucchero, infatti, è substrato dell'enzima fruttochinasi che dà origine a fruttosio-1-fosfato mediante un processo in cui viene consumata una molecola di ATP e prodotta una di ADP e fosfato organico. Questa reazione enzimatica è pressoché irreversibile, per cui ATP non viene rigenerato mentre ADP viene convertito in AMP, che è substrato per la generazione di acido urico (28).
Vediamo ora, sinteticamente, le prove a favore e contro l'esistenza di un rapporto di causa-effetto fra uricemia e malattie cardiovascolari e renali (per una trattazione più dettagliata e per i riferimenti bibliografici si rinvia alla già citata pubblicazione di Feig e Johnson (14).
Ipertensione arteriosa.
L'osservazione che il rilievo di iperuricemia è comune nei soggetti con preipertensione e precede la comparsa di ipertensione suggerisce una possibile causalità del rapporto, che trova conferma nella maggior frequenza di iperuricemia nell'ipertensione essenziale rispetto alle forme secondarie, soprattutto negli adolescenti, mentre la correlazione diviene meno stretta con l'aumentare dell'età e della durata dell'ipertensione. Una dimostrazione sperimentale del ruolo causale dell'acido urico viene dall'osservazione che ratti trattati con un inibitore dell'uricasi sviluppano ipertensione di entità correlata al grado di iperuricemia, e che l'aggiunta di inibitori della xantino-ossidasi o di agenti uricosurici provoca riduzione pressoria. In questo modello sperimentale è stato dimostrato che l'ipertensione è provocata da vasocostrizione renale conseguente a riduzione di NO nell'endotelio e ad attivazione del sistema renina-angiotensina. Nei ratti resi iperuricemici si sviluppa, nel tempo, un danno microvascolare simile a quello arteriolosclerotico tipico dell'ipertensione essenziale, danno che si osserva anche se i valori pressori vengono controllati farmacologicamente. In colture di miocellule vascolari, inoltre, l'acido urico induce proliferazione, infiammazione, stress ossidativo e attivazione del sistema renina-angiotensina. A queste osservazioni fa riscontro, nell'uomo, il rilievo che l'entità dell'uricemia è correlata con il grado di disfunzione endoteliale e con la concentrazione plasmatica di renina.
In adolescenti ipertesi e iperuricemici il trattamento con Allopurinolo a confronto con placebo determina, insieme ad una significativa riduzione dell'uricemia, una altrettanto significativa riduzione pressoria la cui entità è analoga a quella ottenuta con i comuni antiipertensivi.
Sindrome metabolica.
L'iperuricemia spesso osservata in soggetti con sindrome metabolica viene attribuita all'iperinsulinismo, poiché insulina riduce l'escrezione renale di acido urico. D'altra parte l'iperuricemia spesso precede la comparsa di iperinsulinismo, di obesità e di diabete. Le prove più convincenti di un ruolo dell'acido urico nello sviluppo della sindrome metabolica provengono da studi sperimentali, che dimostrano come l'iperuricemia induce nel ratto disfunzione endoteliale e che questa è prevenuta dal trattamento con Allopurinolo. Altre osservazioni indicano che l'iperuricemia determina alterazioni infiammatorie ed ossidative negli adipociti; inoltre l'enzima xantina ossidoreduttasi, che trasforma la xantina in acido urico, è espressa negli adipociti e riveste un ruolo fondamentale nell'adipogenesi.
Nefropatie
In studi sperimentali è stato dimostrato che concentrazioni elevare di acido urico sono in grado di provocare danno renale o di aggravare una preesistente nefropatia anche in assenza di deposizioni di cristalli di urato. I danni consistono in glomerulosclerosi, fibrosi interstiziale e danno arteriolare. Queste alterazioni sono analoghe a quelle che si osservano nella nefropatia gottosa, dalla quale si differenziano solo per l'assenza di cristalli di urato; l'origine sembra costituita un danno arteriolare preglomerulare che impedisce l'autoregolazione del flusso sanguigno determinando ipertensione glomerulare. La responsabilità dell'iperuricemia nella patogenesi del danno renale è suggerita anche da alcuni studi epidemiologici: essa è infatti predittiva di albuminuria e insufficienza renale in soggetti con normale funzione renale e si associa alla diminuzione del filtrato glomerulare in soggetti con diabete mellito tipo 1; per contro non risulta predittiva nei confronti dell'evoluzione di nefropatie croniche preesistenti. Comunque, la riduzione farmacologica dell'uricemia può rallentare la progressione del danno renale, e la sospensione del trattamento è seguita da peggioramento dell'ipertensione arteriosa e da accelerata caduta del filtrato glomerulare.
Altre condizioni cardiovascolari
Varie ricerche hanno portato prove di una associazione tra iperuricemia e vasculopatie periferiche, carotidee e coronariche e con la comparsa di ictus, di preeclampsia e di demenza vascolare; l'associazione appare particolarmente stretta nei soggetti ad alto rischio cardiovascolare e nelle donne. Inoltre, una parte dei benefici cardiovascolari osservati negli studi LIFE e GRACE, condotti con l'uso di Losartan e rispettivamente di Atorvastatina, sono stati attribuiti alla capacità di questi due farmaci di ridurre l'uricemia.
Nonostante le osservazioni fin qui sinteticamente riportate, il ruolo dell'acido urico nella patogenesi delle malattie cardiovascolari non può considerarsi accertato. Le limitazioni più rilevanti riguardano la insufficiente numerosità di molti studi clinici, la selezione dei soggetti trattati e il fatto che i vantaggi osservati durante trattamento con inibitori della xantino-ossidasi non sono stati rilevati anche nei soggetti trattati con altri farmaci ipouricemizzanti; osservazione quest'ultima che potrebbe far attribuire ai primi la capacità di agire sull'acido urico intracellulare e quindi svolgere con questo meccanismo un'azione benefica sulla funzione endoteliale. Restano poi da chiarire meglio le molteplici funzioni biologiche dell'acido urico, che in alcune condizioni può svolgere azione pro-ossidante e antiipertensiva.
Il problema dell'iperuricemia asintomatica
E' attualmente sempre più frequente, soprattutto in soggetti che presentano affezioni facenti parte della sindrome metabolica, il riscontro di valori uricemici elevati. Si pone in questi casi la necessità di stabilire se sia opportuno iniziare un trattamento farmacologico e quindi di valutare i possibili benefici a fronte dei rischi di un trattamento ipouricemizzante a tempo indefinito.
A questo fine, il rilievo di iperuricemia persistente in un soggetto fino a quel momento asintomatico richiede una completa valutazione clinica e biochimica volta a identificare se il soggetto stesso sia ad alto rischio di artrite gottosa, di tofi o di litiasi urinaria; inoltre, se l'iperuricemia sia il segno di una malattia o di una esposizione a farmaci sostituibili o a sostanze tossiche eliminabili. Devono perciò essere ricercate malattie mielo- e linfoproliferative, psoriasi, deficit di Vitamina B12, preeclampsia ed esposizione al piombo. Una volta escluse queste condizioni devono essere misurati creatinina e acido urico nelle urine di 24 ore mentre il paziente segue una dieta standard evitando alcolici e farmaci che alterino il metabolismo purinico. Se la funzione renale è conservata, queste misurazioni permettono di stabilire se vi è iperescrezione di acido urico (uricuria superiore a 800 mg/die o a 12 mg/Kg/die), ovvero se l'uricuria è normale. In quest'ultimo caso si tratta di un soggetto ipoescretore in cui la "normalità" dell'uricuria esprime la necessità di una più elevata uricemia perché l'escrezione possa essere pari alla produzione. In questa condizione, infatti, il calcolo della clearance dell'acido urico darà risultato patologicamente ridotto.
La distinzione fra iperproduzione e ipoescrezione faciliterà la diagnosi eziologica dell'iperuricemia e guiderà il trattamento. L'escrezione frazionale dell'acido urico sul campione delle 24 ore [(uricuria x creatininemia / uricemia x creatininuria) x 100], se inferiore a 6%, permetterà di porre diagnosi di ipoescrezione.
In caso di iperuricuria la raccolta delle urine di 24 ore va ripetuta dopo 4 giorni di dieta isocalorica ipopurinica contenente 1 g/Kg di proteine del latte escludendo alcolici, carne, pesce, fruttosio e farmaci che influenzano il metabolismo purinico. Se l'uricuria resta superiore a 670 mg/die l'iperuricemia potrà essere attribuita a difetti enzimatici o ad aumentato ricambio cellulare; se scende a valori normali sarà invece confermata un'origine alimentare.
Mancando a tutt'oggi ogni certezza sulla responsabilità dell'iperuricemia nella patogenesi delle già ricordate condizioni non dipendenti dalla deposizione di cristalli di urato,un trattamento farmacologico dell'iperuricemia asintomatica appare giustificato solo nei rari soggetti con persistenti valori uricemici superiori a 13 mg/dL nell'uomo e 10 mg/dL nella donna per il rischio nefrotossico che comportano, escludendo i casi in cui l'iperuricemia è provocata da ipoperfusione renale secondaria a insufficienza cardiaca. Costituisce indicazione al trattamento anche una uricuria eccedente i 1.100 mg/die per l'elevato rischio di calcolosi, ma in questi casi il primo provvedimento consiste nella restrizione delle purine nella dieta e solo in caso di insuccesso della somministrazione di farmaci ipouricemizzanti, che deve mirare a portare l'uricuria a meno di 800 mg/die. Altra indicazione al trattamento è costituita dai casi in cui iperuricuria sia secondaria a radio- o chemioterapia (5, 23, 41, 42).
Indicazioni al trattamento farmacologico da valutare caso per caso possono essere rappresentate da familiarità gottosa con insorgenza dei sintomi in giovane età, dalla necessità di uso continuo di diuretici o di ciclosporina e dalla incapacità di osservare le restrizioni dietetiche.
Trattamento dell'attacco gottoso.
Vari farmaci sono in grado di accelerare la scomparsa dei sintomi, che in assenza di trattamento possono richiedere vari giorni o addirittura settimane per regredire. Le molecole più utilizzate sono i FANS e la Colchicina. Ovviamente da evitare l'uso di inibitori della xantina ossidasi, che peggiorerebbero le manifestazioni infiammatorie.
FANS
I vari FANS (ad eccezione di acido acetilsalicilico, che riduce l'uricuria a dosi fino a 3 g/die e la promuove se somministrato a dosi più elevate), compresi gli inibitori di COX-2, mostrano una efficacia equivalente, con riduzione del dolore entro poche ore dall'inizio del trattamento. Tra le molecole più ampiamente utilizzate sono Naprossene, 500 mg b.i.d. e Indometacina, 50 mg t.i.d. L'alternativa offerta dalla Colchicina consiglia di evitare i FANS in presenza di controindicazioni cardiovascolari, renali o digestive; nel caso di queste ultime si può preferire comunque un FANS inibitore di COX-2 o l'aggiunta di un inibitore della pompa protonica (37).
Colchicina
La colchicina è particolarmente efficace se somministrata precocemente, ma l'effetto benefico è molto spesso accompagnato o anche preceduto da diarrea e/o vomito, che si manifestano entro 24 ore dall'inizio del trattamento e precedono la riduzione dei sintomi. La dose abitualmente impiegata è di 2-4 mg/die, che poi viene ridotta progressivamente fino a sospensione quando i sintomi sono regrediti (1, 46).
L'impiego prolungato di Colchicina a dosi ridotte, utile per prevenire gli attacchi all'inizia di una terapia ipouricemizzante. richiede vigilanza su eventuali effetti tossici (debolezza muscolare, aumento CPK, depressione midollare, insufficienza renale). Predispongono alla tossicità l'età avanzata, l'insufficienza renale e le interazioni con farmaci quali Eritromicina, Claritromicina, Simvastatina e Ciclosporina, che riducono l'eliminazione di Colchicina ostacolandone la biotrasfdormazione. (46).
Glicocorticoidi.
I glicocorticoidi sono utili in caso di controindicazioni all'impiego dei FANS e della colchicina, cioè in presenza di: scompenso cardiaco, ipertensione non controllata, insufficienza renale, ulcera peptica, diatesi emorragica, terapia anticoagulante e intolleranza o mancata risposta a FANS o Colchicina. Le dosi abitualmente efficaci sono 25 – 50 mg di prednisone (o dosi equivalenti di altre molecole) al giorno per uno – due giorni e successiva riduzione fino a sospensione dopo sette – dieci giorni. Gli effetti sono analoghi a quelli ottenuti con i FANS, ma le ricadute dopo sospensione del trattamento sono più frequenti. L'infiltrazione intraarticolare con forme deposito può essere considerata in casi di interessamento di una singola articolazione (22).
Le recenti acquisizioni sul meccanismo flogogeno dei cristalli di urato hanno indotto a sperimentare l'effetto di un antagonista ricombinante di IL-1 (Anakinra) , che è apparso efficace e ben tollerato; analoghi risultati sono riportati con l'uso di un bloccante del recettore di IL-1 (Rilonacept) (35, 38)
Prevenzione delle ricorrenze gottose
L'eccesso ponderale è fattore di rischio per la gotta, e il rischio si riduce con il dimagramento (7). Oltre alla riduzione del peso, la dieta povera di purine può ridurre l'uricuria di 200-400 mg/die; ma la diminuzione dell'uricemia non supera in genere 1 mg/dL e una tale dieta è sgradevole e comunque poco utile nei pazienti con normali abitudini alimentari. In questi soggetti una alimentazione con elevato contenuto proteico, ridotto contenuto in grassi saturi e sostituzione dei glicidi semplici con quelli complessi determina una netta riduzione dell'uricemia e degli attacchi gottosi. Questo risultato richiede però che la quota proteica sia rappresentata soprattutto da latticini a basso contenuto lipidico e non da carne o pesce (6,10. Le diete ipoproteiche trovano invece migliore indicazione in presenza di insufficienza renale. Anche il consumo di bevande dolcificate con fruttosio va evitato, data la già ricordata capacità di questo zucchero di favorire la produzione di acido urico. Analoga limitazione deve riguardare liquori e birra, mentre l'effetto del vino appare irrilevante (8).
Sia l'ipertensione essenziale sia l'uso di diuretici (tiazidici e dell'ansa) si associano con iperuricemia e gotta. Il rischio di gotta negli ipertesi è più che doppio rispetto ai normotesi, indipendentemente dall'uso di diuretici, mentre gli ipertesi in trattamento diuretico presentano un rischio di gotta modesto ma comunque maggiore rispetto a quelli non trattati con diuretici (7). L'aumento dell'uricemia con i comuni tiazidici è dose-dipendente e viene ridotto dal concomitante uso di ACE-inibitori o di inibitori recettoriali, in particolare Losartan, che esplica un modesto ma significativo effetto uricosurico (45).
Trattamento farmacologico
L'uso di farmaci si rende necessario in casi di soggetti che presentano attacchi gottosi frequenti e/o intensi e/o prolungati, di segni clinici o radiologici di artropatia gottosa, di tofi sottocutanei o ossei, di insufficienza renale, di urolitiasi ricorrente e di uricuria superiore a 1.100 mg/die in soggetti giovani. L'obiettivo è quello di raggiungere e mantenere l'uricemia a meno di 6 mg/dL o, in presenza di tofi, a meno di 5 mg/dL. Il trattamento ipouricemizzante va iniziato dopo la fine della fase infiammatoria per evitare possibili peggioramenti a deve essere continuato a tempo indeterminato.
La riduzione dell'uricemia può essere ottenuta in due modi: facendo aumentare l'escrezione renale dell'acido urico o riducendone la produzione. Candidati alla prima modalità di trattamento potrebbero essere la maggioranza dei soggetti con iperuricemia, dato che nella grandissima maggioranza dei casi questa è riconducibile ad ipoescrezione (che comunque deve essere confermata dal rilievo di uricuria normale o bassa in presenza di iperuricemia). Il trattamento uricosurico è però attuabile solo in soggetti con normale funzione renale e assenza di urolitiasi ed è comunque gravato dal rischio di favorire la formazione di calcoli e la nefropatia uratica. I farmaci capaci di promuovere l'escrezione urica sono Probenecid, Benzbromarone (entrambi non disponibili in Italia) e Sulfinpirazone. Quest'ultimo (Enturen cp 400 mg), che come gli altri può provocare reazioni cutanee, intolleranza digestiva e interazioni per interferenza con i sistemi di trasporto tubulare di numerosi farmaci anionici, può essere utilizzato in dosi fino a 800 mg/die iniziando con 100 mg/die. Altre molecole dotate di effetto uricosurico, peraltro modesto, sono Losartan, Fenofibrato e Vitamina C (12, 20, 45). Anche se il trattamento con uricosurici sarebbe appropriato per una ampia proporzione di pazienti, esso è ben poco utilizzato per gli inconvenienti cui questi farmaci possono esporre e, in Italia, per la limitata disponibilità di uricosurici. D'altra parte la riduzione della produzione di acido urico con Allopurinolo si dimostra efficace sia negli iper- che negli ipoescretori ed è di fatto il trattamento abituale del'iperuricemia.
Allopurinolo, così come il suo metabolita attivo Ossipurinolo, è un analogo purinico che inibisce competitivamente l'enzima xantina ossidasi arrestando il metabolismo delle purine alla formazione di ipoxantina e di xantina, che vengono eliminate. La dose giornaliera necessaria per portare l'uricemia ai valori desiderati è compresa tra 100 e 600 mg. L'effetto inizia entro 2 giorni e si stabilizza in una-due settimane; la stabilizzazione è di regola più lenta nei soggetti con gotta tofacea. All'efficacia di Allopurinolo fanno riscontro effetti avversi principalmente digestivi (nausea, vomito, diarrea), dermatologici (eruzioni cutanee ma anche casi di necrolisi epidermica tossica e di sindrome di Stevens-Johnson, che sembrano appannaggio dei soggetti con aplotipo di istocompatibilità HLA-B5801) ed ematologici (leuco- e trombocitopenia). Molto rara (0,1%) ma grave (letalità 25%) è una sindrome da ipersensibilità, che sembra favorita dalla presenza di insufficienza renale e dall'uso di diuretici (19, 33, 39) Altri possibili effetti avversi sono vasculiti e nefrite interstiziale; sono segnalati casi di urolitiasi e di cristalluria (cristalli di xantina e di ossipurinolo) in soggetti con uricuria particolarmente elevata. Allopurinolo può essere inoltre causa di interazioni farmacologiche, rappresentate dal potenziamento degli effetti di Azatioprina e di 6-mercaptopurina (che sono in parte degradate dalla xantina ossidasi) e da aumentato rischio di eruzione cutanea da Ampicillina. L'elevata quota del metabolita attivo Ossipurinolo eliminata dal rene impone una netta riduzione della dose in presenza di insufficienza renale.
Tab. II
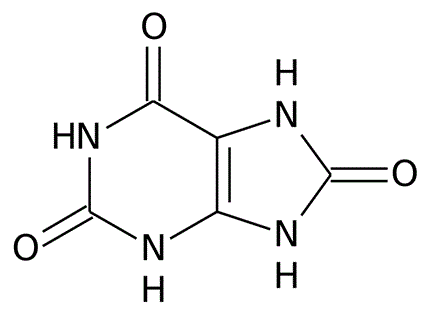
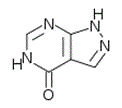
| Acido urico | Allopurinolo | Febuxostat |
 |
 |
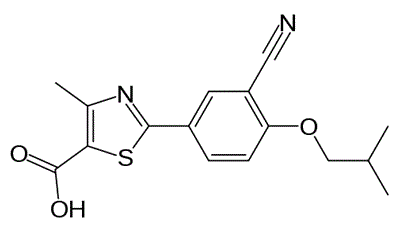 |
Un nuovo inibitore selettivo di xantina ossidasi, Febuxostat, è stato approvato da EMEA nel 2008 e dalla FDA nel 2009 e sarà presto disponibile in Italia (Adenuric® Menarini). Questa molecola, che a differenza di Allopurinolo non è un analogo purinico (Tab. II), alla dose giornaliera di 80 e di 120 mg ha mostrato una capacità ipouricemizzante superiore a quella di Allopurinolo, 300 mg/die. L'efficacia è significativamente ridotta in presenza di insufficienza epatica. Gli effetti avversi sono rappresentati da dispepsia, eruzioni cutanee, artralgie e aumento delle transaminasi. Le interazioni farmacologiche riguardano, come per Allopurinolo, una rallentata biotrasformazione di Azatioprina e di 6-mercaptopurina; anche la biotrasformazione di Teofillina viene rallentata (4, 32). Non sono ancora definite le eventuali limitazioni all'uso imposte da gravi alterazioni della funzione epatica o renale, mentre lievi deficit di tali funzioni appaiono ininfluenti sulla cinetica di Febuxostat.
Le differenze farmacocinetiche tra Allopurinolo e Febuxostat sono riassunte in tabella 3.
tab. III

Una differenza fra Allopurinolo e Febuxostat che assume notevole importanza data la necessità di somministrare questi farmaci per lunghi periodi di tempo è rappresentata dal costo. Un paragone in Euro non è possibile, dato che il prezzo in Italia non è stato ancora fissato; ma negli USA il costo di un mese di trattamento con Febuxostat a dose standard (40 mg/die) è circa 160 $, mentre la spesa per Allopurinolo (300 mg/die) è circa 40 $ per il preparato brand e circa 15 $ per il "generico".
Al momento attuale la scelta fra Allopurinolo e Febuxostat deve essere guidata sia da criteri clinici (presenza di insufficienza renale, intolleranza o inefficacia di Allopurinolo), sia da ragioni economiche. Si deve anche ricordare che l'esperienza clinica con Febuxostat non è ancora paragonabile a quella acquisita in quasi mezzo secolo di uso di Allopurinolo, che appare ancora come il primo farmaco da considerare per ridurre l'uricemia.
Quando la riduzione dell'uricemia non può essere ottenuta inibendone la produzione o favorendone l'eliminazione per intolleranza ai farmaci o per inefficacia dei farmaci stessi, ovvero quando l'obiettivo debba essere raggiunto rapidamente o ancora quando si preveda una improvvisa grave iperuricemia come nel caso di trattamenti citolitici, si può ricorrere all'impiego dell'uricasi (Uricozyme®), estratto dalle colture di Apergillus flavus, disponibile solo per uso ospedaliero. Il trattamento delle forme refrattarie di gotta e della nefropatia urica acuta si potrà in futuro giovare della Uricasi ricombinante legata a polietilenglicole (PEG-uricasi), della quale è stato recentemente completato uno studio in fase 2 presso la Duke University statunitense. Il legame al polietilenglicole (pegilazione), già utilizzato per altri farmaci biologici come Interferone, prolunga l'effetto e riduce l'immunogenicità della sostanza legata rendendone più agevole e sicuro l'impiego. La somministrazione intramuscolare o endovenosa di PEG-uricasi in dosi comprese fra 1 e 24 mg è risultata capace di determinare profonde e prolungate riduzioni dose-dipendenti dell'uricemia, che però si accompagnano spesso a reazioni locali in sede di iniezione e generali dopo infusione endovenosa (17, 36).
In base alle attuali conoscenze i suggerimenti che si possono dare per il trattamento di un paziente che ha superato un attacco gottoso sono i seguenti:
- una terapia farmacologica ipouricemizzante è raccomandata in tutti i soggetti con frequenti attacchi gottosi, segni clinici o radiologici di artrite, tofi, insufficienza renale, nefrolitiasi, uricuria superiore a 1.100 mg/die;
- la dieta (se necessario ipocalorica) deve avere elevato contenuto proteico da ottenersi con derivati magri del latte ed esclusione di carne e pesce; i glicidi raffinati devono essere sostituiti con quelli complessi; deve essere ridotto il contenuto in grassi saturi; devono essere evitati birra e liquori nonché bevande dolcificate con fruttosio;
- in presenza di ipertensione l'uso di basse dosi di diuretici tiazidici non ostacola significativamente l'effetto dei farmaci ipouricemizzanti e può essere consentito; utile l'uso di Losartan per il suo effetto uricosurico;
- la terapia farmacologica deve mirare a ridurre l'uricemia a meno di 6 mg/dL, evitando una velocità di riduzione superiore a 0,5 mg/dL al mese; l'ottenimento di valori inferiori a 5 mg/dL accelera la scomparsa dei tofi;
- il trattamento farmacologico deve essere accompagnato dalla somministrazione profilattica di Colchicina (1-2 mg/die) (o di un FANS in casi di intolleranza), e questa deve essere continuata per sei mesi dopo la normalizzazione dell'uricemia, o più a lungo in caso di tofi persistenti;
- nei soggetti con insufficienza renale le dosi di Allopurinolo devono essere ridotte (fino a 50 mg/die per FG inferiore a 40 mL/min); in questi casi si renderà utile la disponibilità di Febuxostat.
Riassunto
I risultati degli studi di paleontologia genetica sull'assenza di uricasi nell'uomo e nelle grandi scimmie, il progressivo aumento dell'uricemia nei paesi occidentali, le responsabilità dell'alimentazione, le ipotesi su un rapporto di causa-effetto tra iperuricemia e malattie cardiovascolari, la recente disponibilità di nuovi farmaci ipouricemizzanti sono oggetto di questa rassegna nella quale vengono anche presentate le più recenti raccomandazioni sulla prevenzione e sul trattamento dell'iperuricemia e della gotta.
Summary
Uric acide: deeds and misdeeds
The results of genetic anthropology research on the lack of uricase in humans and great apes, the progressive increase of uricemia in western countries, the hypothesis on a link between uric acid and cardiovascular and renal diseases, the recent availability of a new antihyperuricemic drug are the contents of this review, together an up to date on the recommendations for the prevention and treatment of hyperuricemia and gout.
BIBLIOGRAFIA
- Ahern MJ, Reid C, Gordon TP & al, Does colchicine work? The results of the first controlled study in acute glut. Aust N Z J Med 1987:17,301
- Ames BN, Cathcart R, Schwiers E & al,: Uric acid provides an antioxidant defense in humans against oxidant- and radical-caused aging and cancer, Proc Natl Acad Sci 1981:78,6858
- Andrews NW Membrane repair and immunological danger. EMBO Rep 2005:6,826
- Becker MA, Clinical aspects of monosodium urate monohydrate crystal deposition disease (gout), Rheum Dis Clin North Am 1988:126,14,377
- Becker MA, Schumacher HR Jr, Wortmann RL & al, Febuxostat compared with allopurinol in patients with hyperuricemia and gout. N Engl J Med 2005:353,2450;
- Choi HK, Atkinson K, Karlson EW & al, Purine-rich foods, dairy and protein intake, and the risk of gout in men. N Engl J Med 2004:350,1093
- Choi HK, Atkinson K, Karlson EW & al, Obesity, weight change, hypertension, diuretic use, and risk of gout in men: the health professionals follow-up study Arch Intern Med 2005:165,742
- Choi HK, Atkinson K, Karlson EW & al, Alcohol intake and risk of incident gout in men: a prospective study. Lancet 2004:363,1277)..
- Davies KJ, Sevanian A, Muakkassah-Kelly SF & al: Uric acid-iron ion complexes. A new aspect of the antioxidant functions of uric acid. Biochem J 1986:235,747
- Dessein PH, Shipton EA, Stanwix AE & al, Beneficial effects of weight loss associated with moderate caloric/carbohydrate restriction, and increate proportional intake of protein and unsaturated fat on serum urate and lipoprotein levels in gout: a pilot study. An Rheum Dis 2000:59,539
- Di Giovine FS, Malawista SE, Nuk G & al, Interleukin 1 (IL 1) as a mediator of crystal arthritis . Stimulation of T cells and synovial fibroblast mitogenesis by urate crystal-induced IL1. J Immunol 1978:138,3213
- Feher MD, Hepburn AL, Hogart MB & al, Fenofibrate enhances urate reduction in men treated with Allopurinol for hyperuricemia and gout. Rheumatology 2003:42,321
- Feig DI, Johnson RJ: The role of uric acid in pediatric hypertension. J Ren Nutr 2007:17,79
- Feig DJ, Kang D-H, Johnson RJ: Uric acid and cardiovascular risk, N Engl J Med 2008:359,1811
- Fishberg AM The interpretation of increate blood uric acid in hypertension, Arch Intern Med 1924:34,503
- Freedman DS, Williamson DF, Gunter EW & al, Relation of serum uric acid to mortality and ischemic heart disease: the NHANES I Epidemiologic Follow-up Study, Am J Epidemiol 1995:141,637
- Ganson NJ, Kelly SJ, Scarlett E & al, Control of hyperuricemia in subjects with refractory gout, and induction of antibody against poly(ethylene glycol) (PEG), in a phase I trial of subcutaneous PEGylated urate oxidase. Atrhritis Res Ther 2006:8,R12
- Hall AP, Barry PE, Dawber TR & al, Epidemiology of gout and hyperuricemia: a long-trm population study. Am J Med 1967:42,27
- Hande KR, Noone RM, Stone WJ. Severe allopurinol toxicity. Description and guidelines for prevention in patients with renal insufficiency. Am J Med 1984:76,47
- Huang HY, Appel LJ, Choi MJ & al, The effects of Vitamin C supplementation on serum concentrations of uric acid: results of a randomized controlled trial, Arthritis Rheum 2005:52,1843
- Jacobson BM, The uric acid in the serum of gouty and non-gouty individuals: its determination by Folin’s recent method and its significance in the diagnosis of gout. Ann Intern Med 1938:11,1277
- Janssens HJ, Janssen M, van der Lisdok EH & al, Use of oral prednisolone or naproxen for the treatment of gout arthritis: a double-blind, randomised equivalence trial, Lancet 2008:371,1854.
- Kjellstrand CM, Campbell DC, von Hartitzach B & al, Hyperuricemic acute renal failure, Arch Interrn Med 1974:133,349
- Kuntzing MK, Firenstein BL: Altered uric acid levels and disease state. J Pharmacol Exp Ther 2008:324,1
- Liu-Bryan R, Scott P, Sydlaske A & al, Innate immunity conferred by Toll-like receptors 2 and myeloid differentiation factor 88 expression is pivotal to monosodium urate monohydrate crystal-induced inflammation. Arthritis Rheum 2005:52,2936
- Matzinger R. Danger signals: SOS to the immune system. Curr Opin Immunol 2001:13,114
- Mazzali M, Hugues , Kim YG & al Elevated uric acid increases blood pressure in the rat by a novel crystal-independent mechanism. Hypertension 2001:38,1101
- Nagakawa T, Hu H, ZhariKov S & al, A causal role for uric acid in fructose-induced metabolic syndrome, Am J Physiol Renal Physiol 2006:290,F625
- Pacher P, Beckman JS, Liaudet L: Nitric oxide and peroxynitrite in health and disease, Physiol Rev 2007:87,315
- Roddy E; Zhang W; Doherty M The changing epidemiology of gout. Nat Clin Pract Rheumatol. 2007:3,443
- Shi JE, Evans JE, Rock KL: Molecular identification of a danger signal that alerts the immune system to dying cells. Nature 2003:425,516
- Shumacher HR Jr, Becker MA, Wortmann RL & al, Effects of febuxostat versus allopurinol and placebo in reducing serum urate in subjects with hyperuricemia and gout: a 28-week, phase III, randomized, double-blind, parallel-group trial. Arthritis Rheum. 2008;59,1540
- Singer JZ, Wallace SL. The allopurinolo hypersensitivity syndrome. Unnecessary morbidity and mortality, Arthritis Rheum 1986:29,82
- Skoberne M, Beignon AS, Bhardwaj N. Danger signals. A time and space continuum. Trends Mol Med 2004:10,251
- So A, De Smedt T, Revaz S & al, A pilot study of IL-1 inhibition by anakinra in acute gout. Arthritis Res Ther 2007:9,R28
- Sundy JS, Ganson NJ, Kelly SJ & al, Pharmacokinetics and pharmacodynamics of intravenous PEGylated recombinant mammalian urate oxidase in patients wiyh refractory gout. Arthritis Rheum 2007:56,1021
- Sutaria S, Katbamna R, Underwood M, Effectiveness of interventions for the treatment of acute and prevention of the recurrent gout a systematic review, Rheumatology 2006:45,142.
- Terkeltaub R, Schumacher HR, Sundy J & al, Placebo controller pilot study on Rilonacept Am Coll Rheumatol Meeting 2007, Abstr L2.
- Unsworth J, Blake DR, d’Assis Fonseca AE & al, Desensitisation to Allopurinol: a caution tale. Ann Rheumatol Dis 1987:46,646
- van der Veen Hinton DR, Incardonna F & al, Extensive peroxynitrite activity during progressive stages of central nervous system inflammation, J Neuroimmunol 1997:77,1
- Yü T-F, Urolithiasis in hyperuricemia and gout, J Urol 1981:126,424).
- Yü T-F, Gutman AB, Uric acid nephrolithiasis in gout: predisposing factors, Ann Intern Med 1967:67,1133
- Wallace KL, Riedel AA, Joseph-Ridge H & al, Increasing prevalence of gout and hyperuricemia over 10 years among older adults in a managed care population: J Rheumatol 2004:31,1582
- Watanabe S , King DH, Feig L & al, Uric acid, hominoid evolution, and the pathogenesis of salt-sensitivity. Hypertension 2002:40,355
- Wurzner G, Gerster JC, Chiolero A & al, Comparative effects of Losartan and Irbesartan on serum uric acid in hypertensive patients with hyperuricaemia and gout. J Hypertens 2001:19,1855
- Zhang W, Doherty M, Bardin T & al, EULAR evidence based recommendations for gout. Part II: Management. Report of a task force of the EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT) Ann Rheum Dis 2006:65,1312.











.png)





